VACINA FEBRE AMARELA
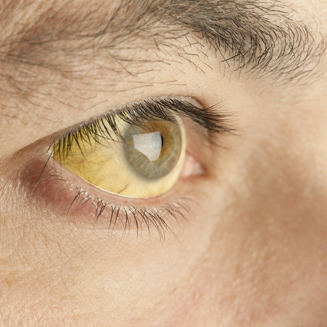
O que previne: Febre amarela.
Do que é feita: Esta vacina é atenuada – composta de vírus vacinal amarílico vivo atenuado (enfraquecido), cultivado em ovo de galinha. Pode conter em sua formulação sacarose, glutamato, sorbitol, gelatina bovina, eritromicina, canamicina, cloridrato de L-histidina, L-alanina, cloreto de sódio e água para injeção.
Indicação: Crianças a partir de 9 meses de idade, adolescentes e adultos que vivem em regiões brasileiras classificadas como áreas de recomendação de vacinação, ou em viagem nacional/internacional de risco para a doença, ou com obrigatoriedade de comprovação da vacinação.
O documento internacional de registro da vacina chama-se Certificado Internacional de Vacinação e Profilaxia (CIVP). Para emissão do CIVP, é preciso procurar os serviços públicos ou privados habilitados para tal, pessoalmente, e apresentar um documento de identidade com foto e a caderneta de vacinação com o registro da vacina.
Contraindicações: Crianças abaixo de 6 meses de idade. Indivíduos infectados pelo HIV, sintomáticos e com imunossupressão grave comprovada por exame de laboratório. Pessoas com imunodepressão grave por doença ou uso de medicação. Pacientes que tenham apresentado doença neurológica desmielinizante no período de seis semanas após a aplicação de dose anterior da vacina.
Mulheres amamentando crianças abaixo de 6 meses de idade. Se a vacinação não puder ser adiada até o bebê completar 6 meses, a mãe deve realizar, antes da vacinação, a ordenha do leite e manter congelado por 28 dias, em freezer ou congelador, para uso durante 28 dias (no mínimo 15 dias), período em que há risco de transmitir o vírus vacinal pelo leite e contaminar o bebê.
Pacientes submetidos a transplante de órgãos. Pacientes com câncer. Pessoas com história de reação anafilática relacionada a substâncias presentes na vacina (ovo de galinha e seus derivados, gelatina bovina ou outras). Pacientes com história pregressa de doenças do timo (miastenia gravis, timoma, casos de ausência de timo ou remoção cirúrgica).
Em princípio há contraindicação para gestantes, mas a administração deve ser analisada de acordo com o grau de risco, por exemplo, na vigência de surtos. A vacinação de indivíduos a partir de 60 anos deve ser evitada, a menos que haja alto risco de infecção.
Esquema de doses: Nas áreas brasileiras com recomendação de vacina:
Rotina: dose única: aos 9 meses idade; Crianças, adolescentes e adultos que já tenham recebido uma dose não precisam ser vacinados novamente. A viajantes para áreas com recomendação ou países que exigem o CIVP é recomendada a comprovação de apenas uma dose na vida. Em situações de exigência da vacinação, a dose deve ter sido aplicada no mínimo dez dias antes da viagem.
Via de aplicação: Subcutânea.
Cuidados antes, durante e após a vacinação: Não são necessários cuidados especiais antes da vacinação. Em caso de febre recomenda-se adiar a vacinação até a melhora.
A administração da vacina em pacientes com lúpus eritematoso sistêmico ou outras doenças autoimunes deve ser avaliada com cuidado, pois pode haver imunossupressão nesses pacientes.
Pacientes transplantados de células de medula óssea também devem ser avaliados, considerando o estado imunológico e o risco epidemiológico, respeitando-se o período mínimo de 24 meses após o transplante. Qualquer sintoma grave e/ou inesperado após a vacinação deve ser notificado ao serviço que a realizou. Todo e qualquer evento adverso grave e/ou inesperado deve ser notificado às autoridades de Saúde.
Efeitos e eventos adversos: Entre os eventos locais, a dor no local de aplicação ocorre em 4% dos adultos vacinados e um pouco menos em crianças pequenas, e essa dor dura um ou dois dias, na forma leve ou moderada. Manifestações gerais, como febre, dor de cabeça e muscular são os eventos mais frequentes e acontecem em cerca de 4% dos que são vacinados na primeira vez e menos de 2% nas segundas doses.
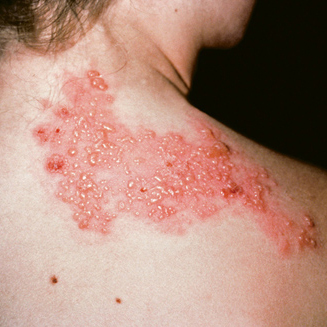
Apesar de muito raros, podem acontecer eventos graves: reações alérgicas, doença neurológica (encefalite, meningite, doenças autoimunes com envolvimento do sistema nervoso central e periférico) e doença em órgãos (infecção pelo vírus vacinal causando danos semelhantes aos da doença).
No Brasil, entre 2007 e 2012, a ocorrência destes eventos graves foi de 0,42 caso por cem mil vacinados. Reações alérgicas como erupções na pele, urticária e asma acontecem com frequência de um caso para 130 mil a 250 mil vacinados. Entre 1999 e 2009, ocorreu anafilaxia na proporção de 0,023 caso para cem mil doses aplicadas. Entre 2007 e 2012, aconteceram 116 casos (0,2 caso em cem mil vacinados) de doença neurológica, principalmente quando se tratava de primeira dose e em idosos. Já a doença nos órgãos, chamada “viscerotrópica”, neste mesmo período, ocorreu em 21 pessoas (0,04 caso em cem mil vacinados).
Onde pode ser encontrada: Nas clínicas privadas de vacinação credenciadas junto à Anvisa e nas Unidades Básicas de Saúde.